Проведение ингаляций через ультразвуковой порт дыхательного контура.
1. Наберите в шприц необходимый лекарственный препарат для ингаляции.
2. Аппарат ИВ Л не выключайте, так как внутри ультразвукового ингалятора есть самогерметизирующиеся клапан, который не допускает утечки и разбрызгивания конденсата при открывании крышки.
3. Откройте крышку небулайзера, залейте необходимое количество лекарственного средства, плотно закройте крышку.
4. Активизируйте работу небулайзера в соответствии с правилами данного аппарата ИВЛ.
Бронхоальвеолярный лаваж (БАЛ).
Забор проб для исследования.
1. Приготовить угловой гофрированный переходник с клапаном отверстия для проведения ФБС, убедиться в его целостности и соответствии соединений данному дыхательному контуру.
2. Произвести замену (в случае загрязнения) или его подсоединение согласно описанному выше алгоритму.
3. Заранее приготовьте и поставьте рядом герметичную емкость утилизации отходов класса В, все необходимые материалы, растворы и лекарственные препараты для проведения БАЛ и забора проб.
4. Провести преоксигенацию пациента в течение 5 минут установив FiO2 100%.
5. Перевести аппарат ИВЛ в режим ожидания и одновременно аккуратно (не повреждая целостность) пережать интубационную трубку зажимом (предпочтительно магистральный зажим).
6. Открыть клапан углового гофрированного переходника и ввести эндоскоп.
7. Снять зажим и незамедлительно возобновить ИВЛ.
8. Выполнить процедуру БАЛ.
9. Забор проб БАЛ для исследования производится в специализированные герметичные стерильные контейнеры.
10. При завершении процедуры не извлекайте эндоскоп одномоментно! Подведите эндоскоп к угловому гофрированному переходнику.
11. Перевести аппарат ИВЛ в режим ожидания и одновременно аккуратно (не повреждая целостность) пережать интубационную трубку зажимом (предпочтительно магистральный зажим) ниже эндоскопа.
12. Извлечь эндоскоп и герметизировать клапан углового гофрированного переходника.
13. Убедиться в герметичности и надёжности соединений.
14. Снять зажим и незамедлительно возобновить ИВЛ.
Выбор режима ИВЛ.
Выбор режима ИВЛ должен заключаться в обеспечении «протективной вентиляции» и максимально возможной поддержки самостоятельного дыхания пациента.
При отсутствии необходимости в седации, вентиляции должен быть в пользу режима с поддержкой самостоятельного дыхания (P-SIMV; V-SIMV; BiPAP; CPAP, PS, ASB,ASV и т.п.).
Базовые настройки аппарата для принудительных вдохов:
- ЧД 15-20 в минуту с соответствующим подбором времени вдоха (Ti), длительности инспираторной паузы и скорости потока для обеспечения соотношения времени вдоха/выдоха (Ti: Te) - 1:1, 5-1:2;
- Установки дыхательного объема (VT) из расчета 4-6 мл/кг ИМТ и с учетом степени поражения легких по данным КТ при типе Н или 7-8 мл/кг ИМТ при типе L;
- VT максимально до 8 мл/кг идеальной массы тела (ИМТ), рекомендуемый 6 мл/кг ИМТ, при выраженном повреждении легочной паренхимы, возможно снижение VT до 4 мл/кг ИМТ.
- Начальный дыхательный объем составляет 6 мл/кг ИМТ; при появлении нежелательных побочных эффектов (например, диссинхрония, pH крови <7,15) допускается увеличение дыхательного объема до 8 мл/кг РВТ. Допустима пермиссивная гиперкапния (описана выше). MV для обеспечения уровня СО2 - 35-45 мм рт.ст., РаО2 55-80 мм рт. ст. и/или SpO2 90-96% при ЧД 15-25/мин (максимально до 35/мин).
PEEP (ПДКВ) в зависимости от уровня оксигенации артериальной крови 10-15-20 см вод. ст. FiO2 - 60-80% в зависимости от уровня оксигенации или сатурации крови.
Использовать ПДКВ не менее 5 см вод. ст. Рассмотреть постепенный перебор указанных ниже комбинаций ПДКВ (PEEP)/FiO2 для достижения целей.
Принципы подбора ПДКВ для детей не отличаются, за исключением того, что детям младше 8 лет требуется более низкое максимальное ПДКВ - 15 см вод. ст., - а пиковое Pplato должно составлять <28 см вод. ст.
Не рекомендуется отключать пациента от аппарата ИВЛ, так как это приводит к потере PEEP, ателектазу и повышению риска инфицирования медицинских работников. Для аспирации секрета из дыхательных путей следует использовать внутриканальные аспирационные катетеры. При необходимости отключения от аппарата ИВЛ (например, при переключении на транспортный аппарат ИВЛ) нужно пережать эндотрахеальную трубку.
Целевое значение Pplato: ≤30 см вод. ст.
- Проверять Pplato при инспираторной паузе 0,5 сек. как минимум каждые 4 часа и после каждого изменения ПДКВ или ДО.
- Если Pplato >30 см вод. ст. или > 28 см вод. ст. у детей: снижать ДО с шагом 1 мл/кг (минимум = 4 мл/кг).
- Если Pplato< 25 см вод. ст., а ДО <6 мл/кг: увеличивать ДО с шагом 1 мл/кг, пока не будет достигнуто Pplato >25 см вод. ст. или ДО = 6 мл/кг.
- Если Pplato< 30 см вод. ст. и происходит накопительное дыхание (breath stacking) или ассинхрония: можно увеличивать ДО с шагом 1 мл/кг до 7-8 мл/кг, если Pplato остается ≤30 см вод. ст.
| ПДКВ ниже / FiO2: выше |
| FiO2 | 0,3 | 0,4 | 0,4 | 0,5 | 0,5 | 0,6 | 0,7 | 0,7 | 0,7 | 0,8 | 0,9 | 0,9 | 0,9 | 1,0 |
| ПДКВ | 5 | 5 | 8 | 8 | 10 | 10 | 10 | 12 | 14 | 14 | 14 | 16 | 18 | 18-24 |
| ПДКВ выше / FiO2: ниже при более тяжелой гипоксемии |
| FiO2 | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 | 0,4 | 0,4 | 0,5 | 0,5 | 0,5-0,8 | 0,8 | 0,9 | 1,0 | 1,0 |
| ПДКВ | 5 | 8 | 10 | 12 | 14 | 14 | 16 | 16 | 18 | 20 | 22 | 22 | 22 | 18-24 |
Лечащий врач должен мониторировать пациента на признак баротравмы при использовании высокого ПДКВ. Для пациентов с ОРДС средней и тяжелой степени предлагается пробное применение более высокого положительного давления в конце выдоха (ПДКВ/РЕЕР) взамен более низкого, что, однако, требует анализа соотношения пользы и рисков. При COVID-19 предлагается индивидуализация PEEP, где во время титрования проводится наблюдение за реакцией пациента (эффект улучшения или ухудшения состояния) и величиной минимального давления вдоха.
Для обеспечения адекватной поддержки самостоятельных вдохов подбирают следующие параметры:
- Чувствительность триггера, чтобы аппарат «видел» каждую попытку пациента вдохнуть. Оценка правильности настройки триггера определяется визуально - аппарат должен отмечать попытку вдоха специальным сигналом.
- Величину давления поддержки (Psupp) для обеспечения расчетного дыхательного объема при самостоятельных вдохах. Можно ориентироваться на частоту самостоятельных вдохов - при слишком высокой частоте следует попробовать увеличить величину поддержки.
При невозможности обеспечить достаточный уровень оксигенации при поддержке самостоятельного дыхания, особенно при психомоторном возбуждении пациента, следует рассмотреть вопрос о необходимости седации для снижения потребности в кислороде и оптимизации механики ИВЛ. Степень седации должна обеспечивать достаточный сон и сохранение самостоятельного дыхания.
При неэффективности седации для обеспечения оптимальной ИВЛ или рекрутмента могут быть кратковременно применены миорелаксанты.
NB!!! Не желательно использовать режимы вентиляции без поддержки самостоятельного дыхания или выключать триггер, так как это может привести к баротравме при не синхронизации с аппаратной вентиляцией.
NB!!! Так же не следует устанавливать ограничение давления вдоха (Рmax) выше 40-50 см вод. ст. для профилактики баротравмы. Только при проведении рекрутмента Ртах может быть повышено до 60 см вод. ст.
Pron-позиция (положение пациента на животе).
NB!!! Не проводить при нестабильной гемодинамике, потребности в высоких дозах инотропной и вазопрессорной поддержки.
Противопоказания [8]:
- повышенное внутричерепное давление >30 мм рт. ст. или церебральное перфузионное давление <60 мм рт. ст.;
- обильное кровохаркание;
- недавно перенесенное хирургическое вмешательство на трахее или стернотомия;
- серьезные травмы лица или хирургические операции на лице;
- лечение по поводу тромбоза глубоких вен в течение менее 2 суток;
- установка искусственного водителя ритма в течение последних 2 дней;
- нестабильные переломы позвоночника, бедренной кости или костей таза;
- СрАД <65 мм рт. ст.;
- беременность;
- установленный плевральный дренаж по передней поверхности грудной клетки с признаками утечки воздуха по дренажу.
Приготовление:
1. Проверить на наличие противопоказаний:
- переломы костей лицевого отдела черепа или костей таза;
- ожоги или открытые раны на вентральной поверхности тела;
- патологии, сопряженные с нестабильностью позвоночника (напр., ревматоидный артрит, травмы);
- патологии, сопряженные с повышенным внутричерепным давлением;
- угрожающие жизни аритмии.
2. Следует учесть возможные нежелательные эффекты положения лежа на животе на дренаж через плевральную трубку.
3. По возможности следует объяснить применяемый прием пациенту или его родственникам.
4. По недавней рентгенограмме грудной клетки убедиться, что конец эндотрахеальной трубки расположен на 2-4 см выше бифуркации трахеи.
5. Путем осмотра убедиться, что эндотрахеальная трубка и все центральные катетеры, а также периферические катетеры большого диаметра, надежно закреплены.
6. Проанализировать, на что именно будут опираться голова, шея и плечевой пояс пациента после переворота в положение лежа на животе. Приготовить подушки, подкладки из пеноматериала и другие опорные средства, которые могут понадобиться.
7. Прекратить питание через зонд, проверить наличие остатков пищи, полностью опорожнить желудок, закрыть зонды для искусственного кормления и желудочные зонды пробками или зажимами.
8. Подготовить оборудование для эндотрахеальной аспирации, повторить процедуру, которую необходимо выполнить, если обильные выделения из дыхательных путей будут мешать вентиляции.
9. Принять решение о перевороте через правый или левый бок.
10. Подготовить все инфузионные катетеры, другие катетеры и трубки для подключения, которые понадобятся, когда пациент будет лежать на животе:
- обеспечить достаточную длину трубок;
- переместить все дренажные мешки на противоположную сторону постели;
- переместить плевральную дренажную трубку между ног;
- переместить инфузионные трубки в сторону головы пациента с противоположной стороны постели.
Порядок выполнения переворота:
1. Разместить одного (или нескольких) людей с обеих сторон кровати (для проведения переворота), а еще одного - в изголовье кровати (чтобы следить за тем, что центральные катетеры и эндотрахеальная трубка не смещались и не перекручивались).
2. Увеличить FiO2 до 1,0 и отметить режим вентиляции, дыхательный объем, минутную вентиляцию, пиковое давление и давление плато в дыхательных путях.
3. Поместить пациента на край кровати, противоположный тому боку, через который будет осуществляться поворот.
4. Поместить новую пеленку на ту сторону кровати, к которой будет обращен пациент в положении лежа на боку. Большая половина пеленки должна свисать вниз.
5. Перевернуть пациента в положении лежа на боку, слегка заведя одноименную руку под грудную клетку. В ходе переворота противоположную руку можно поднять и завести за голову пациента. Либо переворот можно выполнить по схеме «перекатки бревна».
6. Отсоединить отведения и электроды ЭКГ. При необходимости произвести аспирацию дыхательных путей, ротовой полости и носовых проходов.
7. Продолжать переворот в положение лежа на животе.
8. Переместить пациента в центр постели с помощью новой пеленки.
9. Если пациент находится на стандартной больничной койке, повернуть его лицом к аппарату ИВЛ. Убедиться, что во время переворачивания воздуховоды не перекрутились и не сдвинулись. При необходимости произвести аспирацию дыхательных путей.
10. Обеспечить лицу и плечам надлежащую опору, не допуская контакта поддерживающих подкладок с глазницами.
11. Придать рукам пациента комфортное положение. Если пациент не может общаться с внешним миром, то следует избегать вытяжения руки, которое может привести к повреждению плечевого нервного сплетения.
12. Подтвердить отсутствие смещения эндотрахеальной трубки путем оценки сохранившихся прежних значений дыхательного объема, минутной вентиляции, сатурации крови, капнометрии.
13. Поправить положение всех трубок, определить состояние соединений и функционирования систем.
14. Закрепить электроды и отведения ЭКГ на спине.
15. Поместить пациента в обратное положение Тренделенбурга. Кроме того, следует периодически слегка (20-30°) наклонять пациента на бок, меняя сторону каждые 2 часа.
16. Каждую смену необходимо фиксировать результаты тщательного осмотра кожных покровов, обращая особое внимание на вентральные поверхности, на которые приходится нагрузка.
- Эффективно раннее применение!
- Нужно проводить пациентам не только на инвазивной ИВЛ, но и на спонтанном дыхании.
- Продолжительность 12-16 часов!
- Если пациента интубирован (в идеале <48 часов) после 12-24 часов искусственной вентиляции легких, это позволяет оптимизировать лечение.
- Наилучшие результаты достигаются при использовании дыхательных объемов на прогнозируемую массу тела 6 мл/кг и использование нервно-мышечных блокирующих препаратов, если есть признаки десинхронизации с вентилятором.
- Планируйте процедуру за час.
- Проводите таймаут непосредственно перед процедурой (подготовленность пациента, готовность всех членов команды, герметичность контура ИВЛ, наличие необходимых валиков и постельных принадлежностей).
- Проводите преоксигенацию не менее 5 минут.
- Привлекайте минимум 5 участников.
- Определите роли и обязанности каждого участника.
- Соблюдайте положение Фаулера (Фовлера) (30°) после переворота пациента.
- Контролируйте положение подушек/валиков:
- через грудь пациента - позволяя поддерживать грудь и не испытывая давления;
- через таз - обеспечение свободы живота от сдавления;
- под голенями - предотвращение чрезмерного растяжения голеностопного сустава и минимизация давления, оказываемого на колени пациента;
- у беременных женщин возможно применение позиции «лежа на боку».
Методы профилактики ИВЛ-ассоциированной пневмонии.
1. Подберите подходящий размер эндотрахеальной/трахеостомической трубки.
2. Используйте эндотрахеальную/трахеостомическую трубку с подслизистым всасыванием. Конденсат утилизируйте в закрытый контейнер, содержащий предварительно приготовленный дезинфицирующий хлорсодержащий раствор
3. Установите эндотрахеальную трубку на нужную глубину, хорошо закрепите и избегайте натяжения и травмирования мягких тканей.
2. Поддерживайте давление в манжете эндотрахеальной/трахеостомической трубки на уровне 30-35 см вод. ст. и проверяйте это каждые 4 часа;
3. Своевременно санируйте выделения и соблюдайте гигиену полости рта, зубов и носа пациента.
4. Подросткам и взрослым предпочтительно выполнять оротрахеальную, а не назотрахеальную интубацию.
5. Пациент должен находиться в положении полулежа (спинка кровати поднята на 30-45°).
6. Используйте замкнутую систему аспирации; периодически вымывайте и удаляйте конденсат из трубок.
7. Заменяйте тепловлагообменник при его неисправности (износа), загрязнении или каждые 5-7 дней.
Снижение частоты случаев катетер-ассоциированной инфекции кровотока.
- Используйте контрольный перечень шагов, проверяемый наблюдателем в режиме реального времени, в целях обеспечения стерильной установки катетера, а также в качестве ежедневного напоминания о необходимости удаления катетера, если он больше не нужен.
Сокращение частоты возникновения пролежней.
- Переворачивайте пациента каждые 2 часа.
Снижение частоты развития стрессовых язв и желудочно-кишечных кровотечений.
- Начинайте энтеральное питание на ранних этапах (в течение 24-48 часов после поступления пациента в ОРИТ).
- Назначайте блокаторы Н2-гистаминовых рецепторов или ингибиторов протонного насоса пациентам с факторами риска желудочно-кишечного кровотечения. Факторы риска включают искусственную вентиляцию легких в течение >48 часов, коагулопатию, заместительную почечную терапию, заболевания печени, множественные сопутствующие заболевания и более высокий показатель полиорганной недостаточности.
Критерии возможности прекращения респираторной поддержки.
Отлучение пациентки от инвазивной ИВЛ должно начинаться сразу после стабилизации состояния и появлении положительной клинической, лабораторной и рентгенологической динамики.
Проводится с использованием режимов вспомогательной вентиляции с поддержкой давлением - PSV (Pressure Support Ventilation) - вспомогательной вентиляции с поддержкой давлением. Синоним: ASB, СРАР.
Нужно продолжать вентилировать в этом режиме (до 2-3 суток), в динамике постепенно снижая уровень PEEP, в первую очередь, уровень поддерживающего давления Psupp и FiO2 под контролем сатурации, РаО2 и РаСО2, во вторую.
Можно рекомендовать ежедневно уменьшать уровень PEEP (ПДКВ) и Psupp на 1-2 см вод. ст., степень уменьшения FiO2 может быть более медленной, т.к. после отлучения от ИВЛ пациент может и далее получать кислород через назальные канюли или лицевую маску. Без промежуточной вспомогательной вентиляции пациента (тем более, если пациент длительно находился на принудительно-вспомогательной вентиляции) нельзя переводит в режим СРАР или на спонтанное дыхание. Слабость дыхательных мышц! Пациенты с COVID-19 с повреждением легочной паренхимы долго находятся на ИВЛ!
Если пациент готов к самостоятельной вентиляции, далее переходим в режим СРАР (вентиляция легких постоянным положительным давлением).
Показания к отлучению от ИВЛ.
- Ясное сознание;
- Наличие эффективного кашля;
- Положительная динамика основного заболевания (отсутствие фебрильной температуры, выраженной бронхореи);
- Стабильная гемодинамика: САД более 90 мм рт.ст. без вазопрессорной поддержки (допускается введение норадреналин <0,1 мкг/кг/мин, добутамин <5 мкг/кг/мин, дофамин <5 мкг/кг/мин);
- Положительная динамика Rg-картины в легких;
- Приемлемая оксигенация (PaO2/FiO2 >200 при FiO2 <50% и PEEP <10 см вод. ст.);
- Отсутствие необходимости в глубокой седации.
Тест спонтанного дыхания:
1. Самостоятельное дыхание в режиме СРАР с минимальным давлением поддержки (PS) 2-6 см вод. ст. не менее 2-х часов без признаков декомпенсации (тахикардия >120 в мин., изменение АД >20%, тахипноэ более 30, десатурация крови ниже 92%, гиперкапния/гипокапния; нехватка воздуха, беспокойство или слабость, или участие вспомогательной мускулатуры).
2. NB! Режим СРАР с минимальным давлением поддержки (Psupp) необходим только лишь для дополнительного сопротивления в связи с дыханием через трубку. При наличии сомнений в готовности к самостоятельному дыханию, наблюдение может быть продлено более 2-х часов, либо использовать НИВЛ как этап отлучения от ИВЛ или Т-образную трубку.
Дополнительные критерии:
- RSBI (Индекс Тобина (ЧД/ДО) <105 мин. - 1/л;
- индекс РОД < - 4 см вод. ст.,
- PImax (сила вдоха не менее) - 20-25 см вод. ст.);
- Работа дыхания 2,5-5 Дж/мин;
- NTF< - 20.... - 30 см вод. ст.
Алгоритм отлучения пациента от ИВЛ [10]
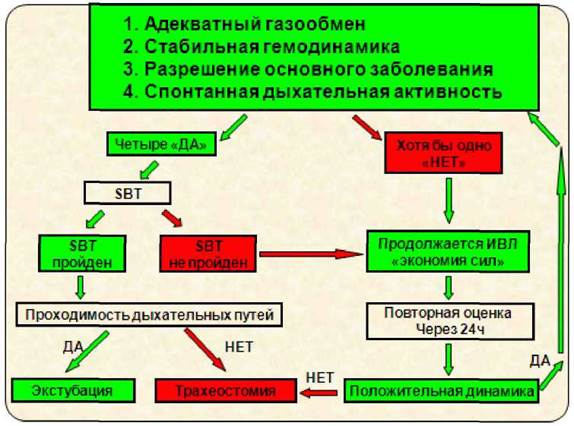
Ранняя реабилитация пациентов в ОРИТ:
При стабилизации состояния пациента и улучшении оксигенации на фоне продолжающейся ИВЛ:
- Уменьшать степень седации;
- Активизировать пациента - сажать на кровати, опуская ноги;
- Удалить назогастральный зонд и больной должен самостоятельно принимать пищу (при наличии трахеостомы).
Варианты седации пациента на ИВЛ:
При необходимости дозы постепенно увеличивают до достижения желаемого терапевтического эффекта. Изучите инструкцию препаратов! При неэффективности одного варианта, можно комбинировать разные варианты.
Доза и комбинация препаратов назначаются в зависимости от того, какой уровень седации по шкале RASS вы преследуете, также на каком режиме ИВЛ находится пациент, какие параметры на ИВЛ, также какие параметры/нарушения ритмы имеются на ЭКГ.
- Пропофол 2-8 мг/кг/час;
- Трамадол 100 мг (каждые 6 часов в/в медленно);
- Дексмедетомидин 0,2-1 мкг/кг/час;
- Галоперидол 5 мг в/в, каждые 6 часов;
- Фентанил 0,005% 20 мл в дозе 0,1 мкг/кг/мин.
(можно + кетамин 500 мг в/в + физ р/р 20 мл, титруя через перфузор 0,5-2 мл/час).
- при необходимости миорелаксанта: Рокурония бромид 20-50 мг/час, использовать строго вместе с седативными препаратами.
Миорелаксация:
У пациентов с ОРДС средней и тяжелой степени (PaO2/FiO2 <150 мм рт.ст.) не следует в рутинном порядке применять нейромышечную блокаду путем непрерывной инфузии мышечных релаксантов. Предлагается предпочесть болюсное введение препаратов для нейромышечной блокады взамен непрерывной инфузии для возможности оценки состоятельности самостоятельного дыхания пациентов в период окончания действия релаксантов.
В случае сохраняющейся асинхронии с аппаратом ИВЛ, при необходимости глубокой седации или сохраняющемся высоком Pplato, возможно задуматься о применении продолжающейся инфузии.
В отличие от обычной практики, показания к миорелаксации у пациентов с инфекцией COVID-19 расширены:
- Интубация трахеи.
- Проведение трахеостомии.
- Усиление терапии у пациентов с ОРДС с индексом оксигенации <150 mmHg на принудительной ИВЛ, крайняя диссинхрония с аппаратом ИВЛ (несмотря на введение седативных и обезболивающих препаратов).
- Проведение рекрутмент манёвра (не рекомендуется рутинно использовать!).
- Перевод пациента находящемуся на ИВЛ в положение «propositioning» Нежелательно непрерывное введение релаксантом (особенно длительного действия) более 48 часов. Более длительное применение может привести к мышечной слабости, особенно дыхательных мышц (в том числе диафрагмы). В результате - продление нахождения пациента на аппаратном дыхании, атрофия дыхательной мускулатуры.
Улучшение легочного кровотока.
У подавляющего большинства пациентов, находящихся на ИВЛ нет признаков классического ОРДС (синдрома «жёстких лёгких»). ИВЛ таких пациентов характеризуется высокой растяжимостью лёгких (Compliance). Основным механизмом, объясняющим наблюдаемую тяжелую гипоксемию, является шунтирование десатурированной крови справа налево, утеря гипоксической регуляции вазоконстрикции, нарушающая вентиляционно-перфузионное соотношение (Va/Q) и вызывающая лёгочную гипертензию [6, 11]. С целью снижения давления в системе лёгочной артерии (ЛА) и улучшения значения Va/Q показана инсуффляция монооксида азота (NО) в дыхательный контур под контролем давления в ЛА (методом ЭхоКГ) и уровня Метгемоглобина (MetHb) в анализе газового состава крови.
В случае необходимости подключения системы подачи NО во время продолжающейся ИВЛ, во избежание контакта медперсонала с аэрозолем контура важно соблюдать следующий алгоритм:
Контур NО приготовить и собрать заранее, включить и произвести калибровку аппарата подачи NО →
Провести преоксигенацию пациента в течение 5 минут установив FiO2 100% →
Перевести аппарат ИВЛ в режим ожидания и одновременно аккуратно (не повреждая целостность) пережать интубационную трубку зажимом (предпочтительно магистральный зажим) →
Разъединить дыхательный контур ИВЛ на уровне влагосборника линии вдоха со стороны пациента →
На это место вставить контур NО, расположив линию подачи NО со стороны аппарата ИВЛ, а линию мониторинга NО со стороны пациента →
Убедиться в герметичности и надёжности соединений →
Снять зажим и незамедлительно возобновить ИВЛ →
Начать подачу NO, снизить FiO2 до прежнего уровня.
Противошоковая терапия у взрослых:
1) Адекватная оксигенация. Пошагово бороться с гипоксемией. При неэффективности кислородотерапии, НИВЛ, в плановом порядке перевести пациента на ИВЛ.
2) Обязательно обеспечение центрального венозного доступа (установить центральный венозный катетер (в одну из центральных вен: внутренняя яремная вена, подключичные вены, бедренные вены)! Рекомендуется использовать ультразвуковую навигацию, для избежания осложнений.
3) Перед тем как назначить инфузионную терапию определите этиологию шока (за счет вазоплегии, вазоспазма и/или за счет первостепенной сердечной коронарогенной или некоронарогенной миокардиальной недостаточности на фоне миокардита, перикардита или острой дистрофии миокарда). Проведите ЭКГ и ЭхоКГ.
- инфузионная терапия показана при отсутствии признаков сердечной недостаточности и при наличии признаков дегидратации и гиповолемии. Кристаллоиды предпочтительны коллоидам. Желательно сбалансированные кристаллоидные растворы. Стартовая инфузия у взрослых. 0,9% раствора натрия хлорида 250-500 мл в первые 15-30 минут, проводя после каждого болюса проверку на предмет признаков перегрузки (резкое повышение ЦВД, ЧСС) [13].
Признаками эффективности инфузионной терапии являются:
- СрАД (>60 мм рт. ст.);
- Восстановление диуреза (>0,5 мл/кг/ч);
- снижение мраморности кожных покровов,
- улучшение времени наполнения капилляров менее 2 сек.;
- нормализация ЧСС;
- восстановление сознания/
4) При недостаточной эффективности инфузионной терапии и признаках вазодилатации (теплые кожные покровы) как вазоактивный препарат первой линии рекомендуется Норадреналин: раствор норэпинефрина 0,05-0,35 мкг/кг/мин (вазоактивные препараты ни в коем случает нельзя вводится в периферическую вену).
Если Норадреналин недоступен, рекомендуется использовать Вазопрессин или Адреналин в качестве вазоактивного средства первой линии, по сравнению с другими вазоактивными веществами, для взрослых с COVID-19 и шоком [13].
Если наряду с вазоплегией имеет место низкий СВ, что особенно характерно при COVID-19 (правожелудочковая недостаточность), предпочтительно назначить дополнительно к Норадреналину Добутамин 5-12 мкг/кг/мин.
По беременным отдельный КП.
* Таблица расчета дозы кардиотоников и вазопрессоров в Приложении 1.1.
Инфузионная терапия.
Инфузионная терапия проводится строго по показаниям, учитывая патологические потери. Целесообразно покрывать суточную физиологическую потребность энтеральным восполнением.
При наличии ОРДС, признаков отека легких в клинической картине целесообразно ограничение жидкостной нагрузки, рассмотреть применение петлевых диуретиков (фуросемид) 0,1-0,5мг/кг/час [13]. Важно контролировать почасовой диурез (с отражением в Карте наблюдения, согласно Приложениям). Целевой темп диуреза - 0,5 мл/кг/час.
Использование методов экстракорпоральной гемокоррекции.
Синдром «цитокинового шторма» считается важным патофизиологическим триггером для прогрессирования COVID-19 специфического повреждения лёгких и развития синдрома полиорганной недостаточности (СПОН) за счет дисфункции иммунной системы, чрезмерным выделением провоспалительных цитокинов, приводящих к диффузному альвеолярному повреждению, образованию гиалиновых мембран, экссудации фибрина и других проявлений травмы легких. В тяжелых случаях «цитокиновый шторм» приводит к дисфункции сердечнососудистой системы, шоку, ДВС-синдрому и, в конечном счете, СПОН.
Около 63% пациентов с COVID-19 имеют протеинурию, 19% имеют повышенный уровень креатинина сыворотки, у 29% тяжелых пациентов развивается острое почечное повреждение (ОПП).
Учитывая особенности патогенеза важное место в составе патогенетического лечения больных тяжелым течением коронавирусной инфекции в ОРИТ должны занимать методы экстракорпоральной гемокоррекции, которые обладают комплексными плейотропными эффектами и позволяют нормализовать уровни цитокинов и других факторов патогенеза, тем самым предотвратить или уменьшить степень тяжести органных нарушений.
Диализная терапия.
При необходимости проведения заместительной почечной терапии (ЗПТ) при ОПП пациент диализируется от 2 до 6 недель, до восстановления функции почек.
При лечении пациентов с ОПП, которые требуют заместительную почечную терапию, следует ответить на следующие вопросы:
- Когда лучше начать лечение ЗПТ?
- Какой вид ЗПТ следует использовать?
- Какой доступ лучше?
- Какой уровень клиренса растворимых веществ следует соблюдать?
Начало ЗПТ.
Абсолютными показаниями к проведению сеансов ЗПТ при ОПП являются:
- Возрастающий уровень азотемии и нарушение диуреза согласно рекомендациям RIFLE, AKIN, KDIGO.
- Клинические проявления уремической интоксикации: asterixis, перикардиальный выпот или энцефалопатия.
- Некоррегируемый метаболический ацидоз (pH <7,1, дефицит оснований - 20 и более ммоль/л, НСОЗ <10 ммоль/л).
- Гиперкалиемия >6,5 ммоль/л и/или выраженные изменения на ЭКГ (брадиаритмия, диссоциация ритма, замедление электрической проводимости тяжелой степени).
- Гипергидратация (анасарка), резистентная к медикаментозной терапии (диуретикам).
К относительным показаниям для проведения сеансов ЗПТ относятся резкое и прогрессирующее увеличение уровня азота мочевины и креатинина крови без очевидных признаков реконвалесценции, когда есть реальная угроза развития клинических проявлений уремической интоксикации.
Показаниями к проведению «почечной поддержки» методами ЗПТ являются: обеспечение полноценного питания, удаление жидкости при застойной сердечной недостаточности, и поддержание адекватного гидробаланса у пациента с полиорганной недостаточностью.
По продолжительности терапии существуют следующие виды ЗПТ:
- интермиттирующие (прерывистые) методики ЗПТ продолжительностью не более 8 часов с перерывом больше, чем длительность очередного сеанса (в среднем 4 часа) (см. МЭС гемодиализ стационарный)
- продленные методы ЗПТ (ПЗПТ), предназначенные для замещения функции почек в течение длительного времени (24 часов и более). ПЗПТ условно разделяются на:
- полупродленные 8-12 часов (см. МЭС полу продленная гемо(диа)фильтрация).
- продленные 12-24 часа (см. МЭС продленная гемо(диа)фильтрация).
- постоянные более суток (см. МЭС постоянная гемо(диа)фильтрация).
Критерии выбора ПЗПТ:
1) Ренальные:
- ОПП / ПОН у больных с тяжелой кардиореспираторной недостаточностью (ОИМ, высокие дозы инотропной поддержки, рецидивирующий интерстициальный отек легких, острое легочное повреждение).
- ОПП / ПОН на фоне высокого гиперкатаболизма (сепсис, панкреатит, мезентериальный тромбоз и др.).
2) Внепочечные показания к ПЗПТ:
- Объемная перегрузка, обеспечение инфузионной терапии.
- Септический шок.
- ОРДС или риск ОРДС.
- Тяжелый панкреатит.
- Массивный рабдомиолиз, ожоговая болезнь.
- Гиперосмолярные комы, преэклампсия беременных.
Методы ЗПТ:
- Гемодиализ интермиттирующий и продленный
- Медленный низкопоточный гемодиализ (МНГД) (slow low effective dialysis - SLED) при лечении ОПП - возможность контроля гидробаланса пациента без колебаний гемодинамики за более короткий промежуток времени (6-8 ч. - 16-24 ч.).
- продленная вено-венозная гемофильтрация (ПГФ),
- продленная вено-венозная гемодиафильтрация (ПВВГДФ).
По рекомендациям KDIGO (2012 г.) при ПЗПТ предлагают использовать в отличие от ИГД регионарную антикоагуляцию цитратом вместо гепарина (если нет противопоказаний). Этот тип антикоагуляции очень полезен у пациентов с гепарин индуцированной тромбоцитопенией и/или с высоким риском кровотечения (ДВС синдром, коагулопатии), когда системная антикоагуляция абсолютно противопоказана.
Продолженная вено-венозная гемофильтрация (ПГФ) представляет собой экстракорпоральный контур с насосом крови, высокопоточным или высокопористым диализатором и замещающей жидкостью.
Продолженная вено-венозная гемодиафильтрация (ПВВГДФ) - экстракорпоральный контур с насосом крови, высокопоточным или высокопористым диализатором, а также с замещающей и диализирующей жидкостями.
По последним данным рекомендуется использовать бикарбонат (не лактат) в качестве буфера в диализате и замещающей жидкости для ЗПТ у пациентов с ОНИ, особенно у пациентов с ОНИ и циркуляторным шоком, также с печеночной недостаточностью и/или лактат ацидозом.
При токсическом ОНИ, сепсисе, печеночной недостаточности с гипербилирубинемией рекомендуется проведение плазмообмена, гемосорбции, плазмосорбции с применением специфического сорбента.
Расчет параметров процедуры гемофильтрации:
Объемы и скорость фильтрации.
А. Одним из главных показателей, который определит эффективность процедуры, является общий объем обмена жидкости, который будет удален из крови пациента, проходящей через фильтр за весь период процедуры.
Для достижения адекватного ответа требуется обмен, равный полному объему всей воды организма. То есть, учитывая, что общий объем воды равен 0,6, данный общепризнанный индекс умножается на массу тела пациента и в результате получается необходимый объем субституата.
Например: пациенту массой 80 кг требуется проведение сеанса гемофильтрации. Необходимый объем обмена: 80 * 0,6 = 48 л. Т.е. расчетный параметр общего обмена, достижение которого будет означать, что процедура выполнена с необходимой эффективностью - 48 л субституата.
Б. Вторым важным показателем является скорость фильтрации, то есть объем жидкости, отсекаемый фильтром из крови пациента за 1 час процедуры.
По рекомендациям KDIGO это 20-25 мл\кг\ч.
Например: пациенту массой 80 кг необходимо рассчитать скорость фильтрации. 80 * 25= 2000 мл\ч.
В. Другие параметры.
1. Длительность процедуры.
Исходя из рассчитанных данных: скорость фильтрации X мл\кг\ч и общий объем обмена Y мл время процедуры равно: T=Y/X ч.
Например: пациенту требуется обменять 48 л со скоростью 2000 мл\ч. Время процедуры: 48000\2000 = 24 ч.
Баланс в длительности процедуры достигается путем расчета целевых параметров и их корректировки в зависимости от конкретной клинической ситуации.
2. Объем ультрафильтрации подбирается индивидуально, в зависимости от показателей диуреза, инфузионной нагрузки, состояния водных секторов. Наилучшим способом, безусловно, является расчет разницы массы тела пациента в «здоровом»состоянии и в тот момент, когда встает проблема удаления лишнего объема жидкости. Также на помощь врачу приходит УЗИ, PiCCO и прочие аппаратные методы, позволяющие рассчитать объем патологической жидкости в различных полостях организма.
3. Антикоагуляция.
Препараты выбора - эноксапарин, фондапаринукс, нефракционированный гепарин.
Рекомендованная дозировка гепарина - 15-20 ЕД\кг\ч.
Коррекция дозы осуществляется индивидуально в зависимости от исходного состояния пациента и контролируется не реже, чем через каждые 2 часа.
Для адекватного контроля используются АЧТВ (удлинение в 1,5 раза) или ACT в диапазоне 150-180 секунд.
Начальная инфузия - 500-1000 ЕД\ч.
Системные глюкокортикостероиды: не рекомендуется рутинно назначать для лечения вирусной пневмонии, если нет других жизненно важных показаний к назначению ГКС. Короткий курс ГКС (5-7 дней) в суточной дозе 1-1,5 мг/кг (по преднизолону) может быть назначен по следующим показаниям [40, 52, 56] (Приложение 8):
- длительная высокая лихорадка более 38°С.
- быстрое прогрессирование процесса в легких с объемом поражения более 50%.
- лимфопения менее 15%.
- выявление консолидации на КТ.
Дексаметазон в дозе 4-12 мг/сут показано пациентам, требующим кислородную поддержку - неинвазивной и инвазивной ИВЛ в течение 10 дней.
Для профилактики развития стрессовых язв желудка и 12-перстной кишки:
Н2-гистаминоблокаторы или ингибиторы протоновой помпы по показаниям в зависимости от возраста.
Контроль гипергликемии: рекомендуется начинать дозированное непрерывное введение инсулина короткого действия, когда 2 последовательных значения уровня глюкозы крови ≥10 ммоль/л. Целью инсулинотерапии является поддержание уровня глюкозы крови на уровне 7,5 ммоль/л. Важным моментом при коррекции гипергликемии является недопущение и избежание гипогликемии.
Приложение 1.1
Таблица расчета дозы кардиотоников и вазопрессоров
(использовать при отсутствии перфузоров с функцией расчета вводимой дозировки препарата).
Ссылка предоставлена автором Логвиненко И.А.
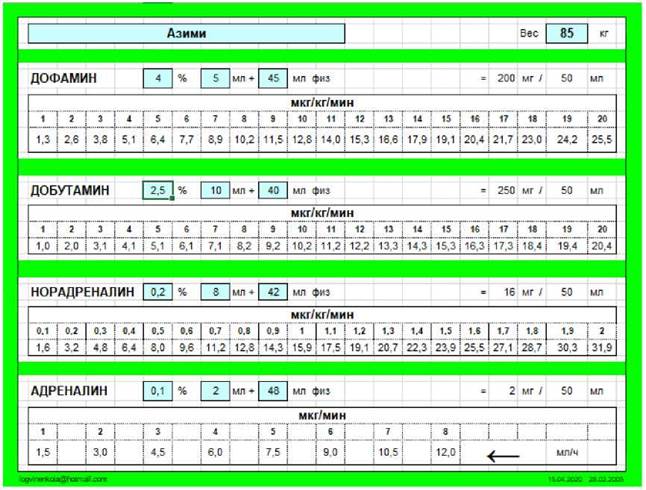
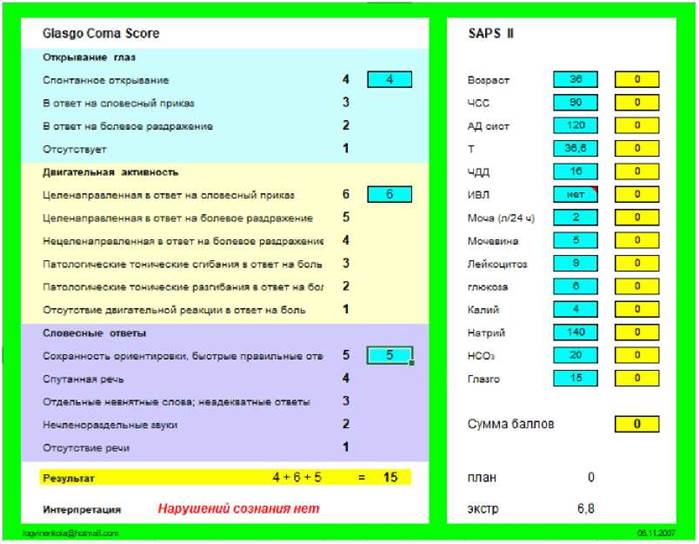
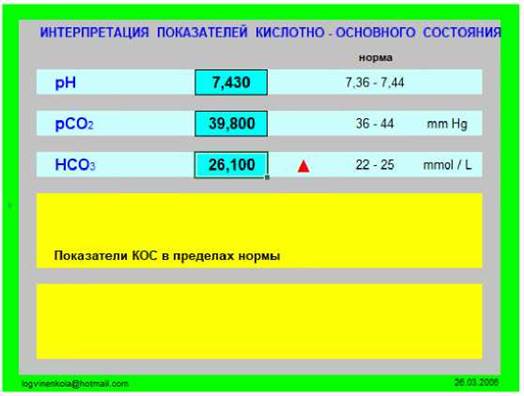
Антикоагулянтная терапия
Приложение 3.
Нутритивная поддержка
Нутритивная поддержка должна проводится всем пациентам за исключением наличия противопоказаний:
- механическая острая кишечная непроходимость;
- высокая кишечная фистула;
- ишемия кишечника;
- несостоятельность межкишечного анастомоза;
- рефрактерный шоковый синдром:
- Гиперлактатемия;
- Метаболический ацидоз - pH 7,2 и менее;

